在医疗器械全生命周期管理中,货架有效期验证和模拟运输验证是确保产品安全性、有效性和稳定性的关键环节,直接关系到患者使用安全与产品市场合规性。
货架有效期(Shelf Life)指医疗器械在规定的储存条件下,能够保持符合注册 / 备案要求的安全性、有效性和质量特性的最长时间,是产品标签、说明书的核心信息之一,也是监管机构重点核查的内容。
模拟运输验证(Simulated Transportation Testing)指通过实验室设备模拟医疗器械在实际流通环节中可能经历的振动、冲击、温湿度变化、堆码压力等环境应力,验证产品包装及内部产品在运输后仍能保持质量合格的试验,核心目标是确保 “最后一公里” 的产品安全。
与医疗器械息息相关的,就是医疗器械的灭菌,目前工业生产主流的医疗器械灭菌方式,主要分为射线灭菌,气体灭菌法,其中环氧乙烷灭菌是当前医疗器械灭菌最主要的灭菌方式之一,应用占50%以上.由于灭菌是一个特殊过程,其输出难以用常规的测量或检测手段加以验证,例如产品的无菌测试为破坏性测试,故必须进行过程确认.
为帮助企业提高应对能力并有效实施相关法规要求,依托YY/T 0681 系列标准;FDA《医疗器械货架有效期指南》,ISO 11607 ,ISO11135-2014,GB18279-2023,AAMI-TIR16等相关标准,计划于2025年10月24日~10月25日,江苏科标与常州依漫联合举办货架有效期验证、模拟运输验证、EO灭菌确认第十八期研讨会。

第十八期研讨班安排如下
研讨会时间:2025年10月24日~2025年10月25日
适合参加人员:医疗器械/卫生用品生产企业从事注册,研发,管理,质量,工艺,法规,供应链相关人员
培训地点:常州市依漫生物科技有限公司厂内(江苏省常州市武进经济开发区长顺路558号)
研讨费用:公益免费
本期名额: 30人,报名成功后会有专人联系。(报名请扫文章末尾二维码)
报名限制:本期每家企业人数限2名,为了更多的企业能了解相关法规,往期未参加的企业将优先安排。
课程安排:8:00~8:50现场签到;培训:上午9:00~下午17:00
联系人:陈老师 18015016921 张小姐:13685202831
注意事项:报名学员提前提交课程内容相关问题,以便在讲课课程中着重讲解,本次报名时限截止日期为2025年10月20日,额满将提前截止。
课程内容
主题1:医疗器械包装系统有效期验证
1、货架有效期验证
2、模拟运输验证
主题2:EO灭菌过程确认
1、相关标准解读
2、灭菌原理及灭菌方法选择
3、灭菌工艺核心要素和影响因素
4、环氧乙烷灭菌设备安装鉴定及运行鉴定
5、环氧乙烷灭菌鉴定PQ
6、环氧乙烷灭菌确认方案和报告编制的要点
7、新版GB18279与老版本差异的解读
8、环氧乙烷灭菌常见问题
主题2:EO灭菌质量相关要点
1、内外审核要点及解答
2、灭菌现场的规范管理
3、委外灭菌供方选择的注意事项
主题四:线上考试
培训合格颁发实训中心上岗证书
培训讲师
1、李明明,江南大学微生物学硕士,江苏科标医学项目负责人。多年医疗器械检测行业经验,专注于医疗器械微生物及物理性能相关检测、医疗器械包装检测、工艺用水检测、洁净区环境检测等。
2、祁闯将,依漫生物技术负责人。生物技术专业/灭菌专家,从事环氧乙烷灭菌行业超过15年,曾主导过国内外知名器械公司灭菌项目。
3、陶乃琦,依漫生物质量负责人/管代。微生物,化学专业/灭菌专家,从业经验超过20年。曾主导过多家公司通过ISO13485审核,CE审核,国内GMP审核,日本、韩国GMP审核。
往期印象

(往期照片:学员讨论)

(往期照片:参观实验室)

(往期照片:现场讨论)

(往期照片:现场讨论)
路线和住宿
一:路线
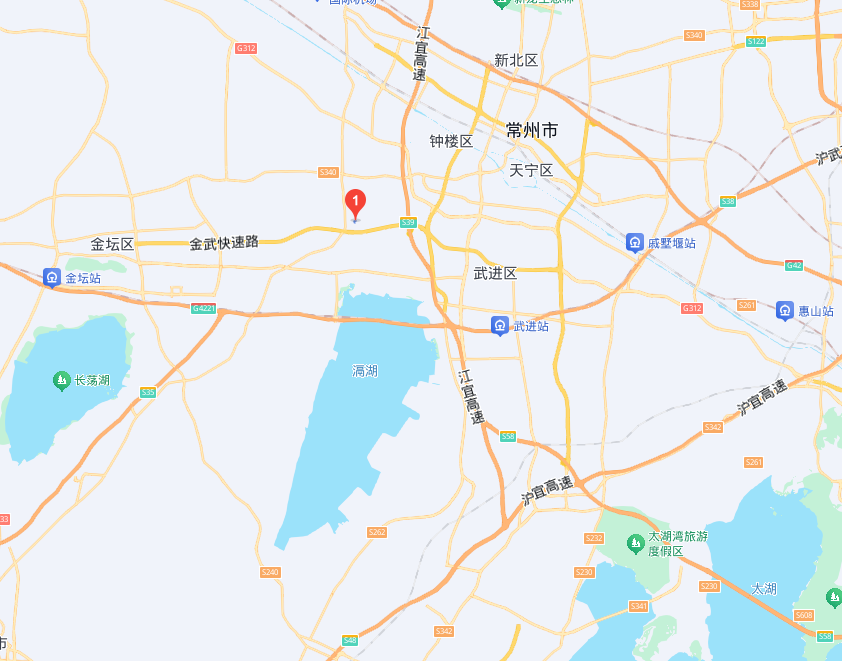
二、住宿
①合作酒店:武进九洲喜来登酒店、都喜富都滨湖酒店
②非合作附近酒店:明都豪格国际酒店、常州名人大酒店、格林豪泰、全季酒店、维也纳酒店等
备注:如预定合作酒店,可以联系张女士(0519-68020290)提前预定,其他酒店可以自行在携程、同程等APP预定。
PS: 报名请扫码

网 址:www.emanmed.com
邮 箱:xxs@emanmed.com
电 话:0519-68020290
手 机:15295010936
地 址:江苏省常州市武进经济开发区长顺路558号
邮 编:213100



